Historia del enlace químico
Los elementos químicos se combinan de diferentes maneras para formar
toda una variedad de compuestos inorgánicos y orgánicos. Hay compuestos
gaseosos, líquidos y sólidos, los hay tóxicos e inocuos, mientras que otros son
altamente benéficos para la salud. Las propiedades de cada compuesto dependen
del tipo de elemento químico que lo forman, el modo cómo se enlazan (tipo de
enlace químico), la forma y geometría de los agregados atómicos (moléculas) y
de cómo estos interactúan entre sí.
El descubrimiento de la naturaleza eléctrica de la materia arrojó
una luz fundamental sobre el concepto del enlace químico. Así Berzelius fue
el primero, en 1812, en dar una explicación a esta cuestión, en cierta medida
con un sentido ya "moderno": sugiere que los átomos se combinarían
entre sí, obedeciendo a una atracción de tipo eléctrico. Es la llamada teoría
dualista del enlace y si bien esta explicación resultaba válida en principio
para los compuestos del mundo mineral, no fue lo mismo cuando se intentó
aplicar a los compuestos orgánicos. Para este tipo de compuestos introducen Frankland
y Kelulé, a partir de 1850, el concepto de valencia que, mas que dar una
explicación al cómo y al porqué se unen los átomos en un compuesto orgánico
atiende más hacer "referencia” a una fuerza interatómica que implica un
numero relacionado con la cantidad de enlaces por los que un átomo podía unirse
a otros.
Determinación de enlace
Un enlace es la unión entre los átomos de un compuesto.
La unión o enlace entre los átomos tiene su origen en la estructura electrónica
de los mismos. La actividad química de los elementos radica en su tendencia a
adquirir, mediante su unión con otros átomos, la configuración de gas noble
(ocho electrones en la capa más externa, salvo el helio que sólo tiene dos),
que es muy estable. Es corriente distinguir tres tipos principales de enlaces
químicos: iónico, covalente y metálico; de los cuales se hablará más
extensamente después. Aunque dichos enlaces tienen propiedades bien definidas,
la clasificación no es rigurosa, existiendo una transición gradual de uno a
otro, lo que permite considerar tipos de enlace intermedios. Gracias a estos
enlaces se forman los compuestos químicos, por ejemplo la sal.
La sal común es un sustancia bien conocida. Es utilizada para
conservar y aderezar alimentos. Nuestra sangre posee casi la misma proporción
de sal que el agua del mar, y es fundamental para mantener muchas de nuestras
funciones vitales. Está formada por un no metal, el cloro y un metal alcalino,
el sodio. Ambos en estado puro son extremadamente peligrosos para el hombre,
sin embargo, forman juntas una sustancia, la sal común, que es inocua en
pequeñas cantidades. Se dice por tanto que han formado un compuesto químico,
una sustancia muy diferente de los elementos que la componen.
Muchas de las sustancias que conocemos están formadas por
uniones de distintos elementos. El azúcar, por ejemplo, está formado por
oxígeno, hidrógeno y carbono. Estos átomos que pierden o ganan electrones para
unirse se transforman en iones, átomos con carga eléctrica. Estos iones se unen
para formar compuestos químicos, y la forma de unirse entre ellos se denomina
enlace químico, del cual se va a hablar en este trabajo.
LEY DE OCTETO
La regla del
octeto establece que los átomos de los elementos se enlazan unos a otros en el
intento de completar su capa de valencia (ultima capa de la electrosfera).
La denominación
“regla del octeto” surgió en razón de la cantidad establecida de electrones
para la estabilidad de un elemento, o sea, el átomo queda estable cuando
presenta en su capa de valencia 8 electrones.

Para alcanzar
tal estabilidad sugerida por la regla del octeto, cada elemento precisa ganar o
perder (compartir) electrones en los enlaces químicos, de esa forma ellos
adquieren ocho electrones en la capa de valencia.
Por ejemplo
tenemos:
Veamos que los
átomos de oxígeno se enlazan para alcanzar la estabilidad sugerida por la regla
del octeto. Los diferentes colores de electrosfera mostrados en la figura nos
ayudan a interpretar lo siguiente:
1 – Átomos de
Oxigeno poseen seis electrones en la capa de valencia (anillo externo en la
figura)
2 – Para
volverse estables precisan contar con ocho electrones. ¿Y como lo logran
entonces?
Comparten dos
electrones (indicado en la unión de los dos anillos), formando una molécula de
gas oxígeno (O2)
La justificativa
para esta regla es que las moléculas o iones, tienden a ser más estables cuando
la capa de electrones externa de cada uno de sus átomos está llena con ocho
electrones (configuración de un gas noble).
Es por ello que
los elementos tienden siempre a formar enlaces en la busqueda de tal
estabilidad.
Excepciones a la
regla del Octeto
Berilio (Be)
Es una excepción
a la regla del Octeto porque es capaz de formar compuestos con dos enlaces
simples, siendo así, se estabiliza con apenas cuatro electrones en la capa de
valencia.
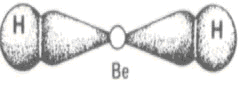
Como el hidrógeno (H) precisa ceder dos electrones para realizar el enlace (H ― Be ― H), el átomo de Berilio (Be) comparte sus electrones y alcanza la estabilidad.
Aluminio (Al)
Es una excepción a la regla del octeto porque alcanza la estabilidad con seis electrones en la capa de valencia. El átomo de aluminio tiende a donar sus electrones y así puede formar tres enlaces simples con otros átomos
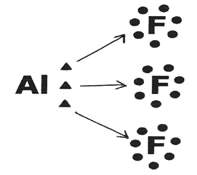
Es una excepción a la regla del octeto porque alcanza la estabilidad con seis electrones en la capa de valencia. El átomo de aluminio tiende a donar sus electrones y así puede formar tres enlaces simples con otros átomos

En este caso, el
Aluminio (Al) formó tres enlaces con tres átomos de Fluor (F)
Boro (B)
Forma sustancias moleculares con tres enlaces simples.
Boro (B)
Forma sustancias moleculares con tres enlaces simples.
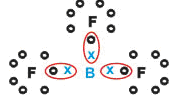
Fijémonos que el Boro (B) tiene la tendencia de donar sus electrones para los átomos de Flúor (F), este si obedece a la regla del Octeto, necesitando sus ocho electrones en la capa de valencia. Como el Boro cede sus electrones, el Flúor se estabiliza con el Octeto formado.
ENERGÍA DE IONIZACIÓN
Es una energía muy elevada para los gases nobles y es necesaria una mayor cantidad de energía.
Las energías de ionización pequeña indican que los e- se arrancan con facilidad.
A medida que aumenta n el e- está más lejos del núcleo, la atracción es menor y por lo tanto, la energía de ionización es menor.
En el mismo periodo aumenta la carga nuclear y la energía de ionización tiene valores más grandes.
AFINIDAD ELECTRÓNICA
La afinidad electrónica de un elemento (AE), puede definirse como:
La cantidad de energía que se absorbe cuando se añade un electrón a un átomo gaseoso aislado para formar un ión de carga 1-
La convención es asignar un valor positivo cuando se absorbe energía y un valor negativo cuando se libera y caso todos los elementos no tienen afinidad por un electrón adicional, por tanto, su afinidad electrónica es igual a cero. La afinidad electrónica de los elementos He y Cloro puede representarse como:
He(g) + e- x He- (g) AE = 0 kj/mol
Cl(g) + e- → Cl- (g) + 349 kj AE = -349 kj/mol
La primera ecuación nos dice que el Helio no admitirá un electrón. La segunda ecuación nos dice que cuando una mol de átomo de cloro gaseoso gana un electrón para formar iones cloruro gaseoso, se libera (exotérmico) 349 kj de energía.
La afinidad electrónica comprende la adición de un electrón a un átomo gaseoso neutro. Así como el proceso por el cual un átomo neutro X gana un electrón.
X(g) + e- →X-(g) (AE)
no es el inverso del proceso de ionización
X+(g) + e- →X(g) ( inverso de EI1)
El primer proceso comienza con un átomo neutro en tanto que el segundo comienza con un ión positivo; por tanto, los valores de EI1 y de la AE no son simplemente iguales pero de signo contrario. En la figura 6.3 vemos que, al recorrer un periódo de la tabla periódica la afinidad electrónica se vuelve, en general,más negativa de izquierda a derecha ( excluyendo a los gases nobles), lo cual significa que casi todos los elementos representativos de los grupos 1A a 7ª muestran gran atracción por un electrón extra de izquierda a derecha. La afinidad electrónica más negativa corresponde a los átomos de los halógenos, cuya configuración electrónica más externa es ns2np5, los cuales forman aniones estables con configuración de gas noble, ns2np6 al ganar un electrón.
Los elementos con afinidad electrónica muy negativa gana electrones con facilidad formando iones negativos (aniones).
La afinidad electrónica es un término preciso y cuantitativo como la energía de ionización, pero es difícil medirla.

VALENCIA
La valencia, es el número de electrones que tiene
un elemento en su último nivel de energía, son los que pone en juego durante
una reacción química o para establecer un enlace con otro elemento. Hay
elementos con más de una valencia, por ello se reemplaza a este concepto con el
de números de oxidación que a fin de cuentas representa lo mismo. A través del
siglo XX, el concepto de valencia ha evolucionado en un amplio rango de
aproximaciones para describir el enlace químico, incluyendo la estructura de Lewis (1916), la teoría del enlace de valencia(1927), la teoría de los orbitales moleculares (1928), la teoría de repulsión de
pares electrónicos de la capa de valencia (1958) y todos los métodos avanzados
de química cuántica.

NUMERO DE OXIDACIÓN
Se denomina número de oxidación a la carga que se le asigna a un átomo cuando los electrones de enlace se distribuyen según ciertas reglas un tanto arbitrarias.
Las reglas son:
Los electrones compartidos por átomos de idéntica electronegatividad se distribuyen en forma equitativa entre ellos.
Los electrones compartidos por átomos de diferente electronegatividad se le asignan al más electronegativo.
Luego de esta distribución se compara el número de electrones con que ha quedado cada átomo con el número que posee el átomo neutro, y ése es el número de oxidación. Éste se escribe, en general, en la parte superior del símbolo atómico y lleva el signo escrito.
Por ejemplo: Vamos a determinar el número de oxidación del Cl en Cl2 y en HCl.
Los dos electrones de enlace se reparten uno para cada átomo, ya que por tratarse de átomos del mismo elemento, obviamente tendrán igual valor de electronegatividad. Cada átomo de Cl queda ahora con 7 electrones de valencia, que son los mismo que tiene el átomo neutro, lo que determina que su número de oxidación sea 0.
Los dos electrones de enlace se le asignan al Cl por ser el átomo de mayor electronegatividad, quedando así, con 8 electrones de valencia, uno más que los del átomo neutro, por lo que su número de oxidación es –1. El H ha quedado sin su único electrón, y su número de oxidación es +1.
De las dos reglas anteriores surge una serie de reglas prácticas que permiten asignar números de oxidación sin necesidad de representar las estructuras de Lewis, las cuales a veces pueden ser complejas o desconocidas
TIPOS DE ENLACE
Como
dijimos al principio, el hecho de que los átomos se combinen o enlacen
para formar nuevas sustancias se explica por la tendencia a conformar
estructuras más estables. De ahí que dichos enlaces químicos sean considerados
como un incremento de estabilidad.
Para
lograr ese estado ideal estable, los átomos pueden utilizar algún método que
les acomode, eligiendo entre: ceder o captar electrones, compartir electrones
con otro átomo o ponerlos en común junto con otros muchos.
De estas
tres posibilidades nacen los tres tipos de enlace químico: iónico, covalente y metálico.
Tomando
como base la diferencia de
electronegatividad entre los
átomos que forman un enlace se puede predecir el tipo de enlace que se formará:
|
Si la
diferencia de electronegatividades es mayor que 2.
|
=
|
se
formará un enlace iónico
|
|
Si la
diferencia de electronegatividades es mayor que 0,5 y menor a 2,0.
|
=
|
el
enlace formado será covalente polar
|
|
Si la
diferencia de electronegatividades es menor a 0,5
|
=
|
el
enlace será covalente puro (o no polar).
|
Enlace
iónico
Cuando una
molécula de una sustancia contiene átomos
de metales y no metales, los electrones son atraídos con más fuerza por los no
metales, que se transforman en iones con carga negativa; los metales, a su vez,
se convierten en iones con carga positiva.
Entonces,
los iones de diferente signo se atraen electrostáticamente, formando enlaces
iónicos.
Este
enlace se origina cuando se transfiere uno o varios electrones de un átomo a
otro. Debido al intercambio electrónico, los átomos se cargan positiva y
negativamente, estableciéndose así una fuerza de atracción electrostática que
los enlaza. Se forma entre dos
átomos con una apreciable diferencia de electronegatividades, los elementos de
los grupos I y II A forman enlaces iónicos con los elementos de los grupos VI y
VII A.
enlace ionico de NaCl
En
general, cuando el compuesto está constituido por un metal y un no-metal y
además la diferencia en electronegatividades es grande, el compuesto es iónico. Es el caso del bromuro de
potasio (KBr).
Propiedades
de un enlace iónico
Los productos
resultantes de un enlace iónico poseen características especiales:
• Son
sólidos de elevado punto de fusión y ebullición.
• La
mayoría son solubles en disolventes polares como el agua.
• La
mayoría son insolubles en disolventes apolares como el benceno o el hexano.
• Las
sustancias iónicas conducen la electricidad cuando están en estado líquido o en
disoluciones acuosas por estar formados por partículas cargadas (iones),
pero no en estado cristalino, porque los iones individuales son demasiado
grandes para moverse libremente a través del cristal.
• Al
intentar deformarlos se rompe el cristal, son frágiles.
Se presenta
cuando se comparten uno o más pares de electrones entre dos átomos cuya
diferencia de electronegatividad es pequeña.
Enlace
covalente apolar (o no polar)
Si los átomos
enlazados son no metales e idénticos (como en N2 o en O2), los electrones
son compartidos por igual por los dos átomos, y el enlace se llama covalente apolar.
Se establece
entre átomos con igual electronegatividad. Átomos del mismo elemento presentan
este tipo de enlace.
Enlace covalente apolar: Molécula de N2
(Usando la Notación de Lewis)
En este enlace
covalente no polar, la densidad electrónica es simétrica con respecto a un
plano perpendicular a la línea entre los dos núcleos. Esto es cierto para todas
las moléculas diatómicas homonucleares (formadas por dos átomos del mismo
elemento) , tales como H2, O2, N2, F2 y Cl2, porque los dos
átomos idénticos tienen electronegatividades idénticas. Por lo que podemos
decir:los enlaces covalentes en todas las moléculas diatómicas homonucleares
deben ser no polares. Por ejemplo, una molécula de dióxido de carbono (CO2)
es lineal con el átomo de carbono al centro y, por lo tanto, debido a su
simetría es covalente apolar.
Enlace
covalente polar
Si los átomos
son no metales pero distintos (como en el óxido nítrico, NO), los electrones
son compartidos en forma desigual y el enlace se llama covalente polar (polar
porque la molécula tiene un polo eléctrico positivo y otro negativo, y
covalente porque los átomos comparten los electrones, aunque sea en forma
desigual).
Se establece
entre átomos con electronegatividades próximas pero no iguales.
Estas
sustancias no conducen la electricidad ni tienen brillo, ductilidad o
maleabilidad.
Veamos un
ejemplo:
¿Qué tipo de
enlace se formará entre H y O?
Según la Tabla de Electronegatividades de
Pauli, el Hidrógeno tiene una electronegatividad
de 2,2 y el Oxígeno 3,44, por lo tanto la diferencia de
electronegatividades será: 3,44 – 2,2 = 1,24.
El resultado
de la operación entrega 1,24 cifra que es menor que 2,0 y mayor que 0,5.
Por lo tanto,
el enlace será covalente polar.
Además, si no se conociera la electronegatividad de los elementos bastaría
saber que son dos no metales distintos para definir su enlace como covalente
polar.
Enlace
covalente coordinado
Se establece
por compartición de electrones entre dos átomos, pero sólo un átomo aporta el
par de electrones compartidos.
Propiedades
de los enlaces covalentes
• Son
gases, líquidos o sólidos de bajo punto de fusión.
• La
mayoría son insolubles en disolventes polares.
• La
mayoría son solubles en disolventes apolares.
• Los
líquidos y sólidos fundidos no conducen la electricidad.
• Las
disoluciones acuosas son malas conductoras de la electricidad porque no
contienen partículas cargadas.
Enlace
metálico
Si los átomos
enlazados son elementos metálicos, el enlace se llama metálico. Los electrones son
compartidos por los átomos, pero pueden moverse a través del sólido
proporcionando conductividad térmica y eléctrica, brillo, maleabilidad y
ductilidad.
Los electrones
que participan en él se mueven libremente, a causa de la poca fuerza de
atracción del núcleo sobre los electrones de su periferia.
Cuando los
electrones son compartidos simétricamente, el enlace puede ser metálico o
covalente apolar; si son compartidos asimétricamente, el enlace es covalente
polar; la transferencia de electrones proporciona enlace iónico. Generalmente,
la tendencia a una distribución desigual de los electrones entre un par de
átomos aumenta cuanto más separados están en la tabla periódica.
Cómo se
forman los enlaces covalentes no polares y polares
Al contrario
de los enlaces iónicos, en los cuales ocurre una transferencia completa de
electrones, el enlace covalente ocurre cuando dos (o más) elementos comparten
electrones.
El enlace
covalente ocurre porque los átomos en el compuesto tienen una tendencia similar
hacia los electrones (generalmente para ganar electrones). Esto ocurre
comúnmente cuando dos no metales se enlazan. Ya que ninguno de los no metales
que participan en el enlace querrá ganar electrones, estos elementos
compartirán electrones para poder llenar sus envolturas de valencia.
Un buen
ejemplo de un enlace covalente es ese que ocurre entre dos átomos de hidrógeno.
Los átomos de
hidrógeno (H) tienen un electrón de valencia en su primera y única capa o
envoltura. Puesto que la capacidad de esta envoltura es de dos electrones, cada
átomo hidrógeno tenderá a captar un segundo electrón.
Enlace covalente apolar entre dos átomos de hidrógeno (H) |
En un esfuerzo
por recoger un segundo electrón, el átomo de hidrógeno reaccionará con átomos H
vecinos para formar el compuesto H2. Ya que el compuesto de
hidrógeno es una combinación de átomos igualados, los átomos compartirán cada
uno de sus electrones individuales, formando así un enlace covalente. De esta
manera, ambos átomos comparten la estabilidad de una envoltura de valencia.
Siempre que
dos átomos del mismo elemento se enlazan (formando moléculas diatómicas
homonucleares), tendremos un enlace no polar.
Otro ejemplo
de enlace covalente apolar (no polar), pero con átomos diferentes, es el metano
(CH4).
La
electronegatividad del carbono es 2,5 y la del hidrógeno es 2,1; la diferencia
entre ellos es de 0,4 (menor de 0,5), por lo que el enlace se considera no
polar. Además, el metano es una molécula muy simétrica, por lo que las pequeñas
diferencias de electronegatividad en sus cuatro enlaces se anulan entre sí.
En cambio, se
forma un enlace polar cuando los electrones son desigualmente compartidos
(permanecen más tiempo cerca de un átomo que del otro) entre dos átomos. Los
enlaces covalentes polares ocurren porque un átomo tiene una mayor afinidad
hacia los electrones que el otro (sin embargo, no tanta como para empujar
completamente los electrones y formar un ión).
Esto quiere
decir que, en un enlace covalente polar los electrones que se enlazan pasarán
un mayor tiempo alrededor del átomo que tiene la mayor afinidad hacia los
electrones. Un buen ejemplo del enlace covalente polar es el enlace hidrógeno -
oxígeno en la molécula de agua.



No hay comentarios:
Publicar un comentario