- Qué entiendes por enlace químico?
- Identifique y defina las propiedades que debe tener todo enlace químico para su formación?
- Qué diferencia encuentras entre número de oxidación y valencia de un elemento?
- Cuales son los diferentes tipos de enlaces que existen definalos y de ejemplos?
- Que entiendes por enlace ionico?
Por enlace químico entiendo que es la fuerza de atracción
mutua entre dos o más átomos que se combinan para formar una molécula. Es un
mecanismo electrónico en el cual se ejercen fuerzas de atracción y separación
en el que se unen los átomos para que pueda adquirir la estructura electrónica
del gas noble más cercano al sistema periódico. Para los diferentes elementos
su objetivo es completar la última fase en su máximo rango.
- Identifique y defina las propiedades que debe tener todo enlace químico para su formación?
Potencial de ionización: (PI) es la energía
mínima requerida para separar un electrón de un átomo o molécula específica a
una distancia tal que no exista interacción electrostática entre el ion y el
electrón.
Afinidad electrónica: La afinidad electrónica (AE) o electroafinidad se define como la energía liberada cuando un átomo gaseoso neutro en su estado fundamental (de mínima energía) captura un electrón y forma un ion mononegativo.
Electronegatividad: La electronegatividad es una medida de la capacidad de un átomo (o de manera menos frecuente un grupo funcional) para atraer a los electrones, cuando forma un enlace químico en una molécula.
Para formar un enlace químico se deben cumplir dos reglas:
La regla del octeto: Los átomos se combinan mediante procesos que implican pérdida, ganancia o compartimiento de electrones de tal forma que adquieran la configuración de ocho electrones en su último nivel; esto se conoce como regla del octeto. Sabemos que los gases nobles tienen ocho electrones en su nivel electrónico más interno (excepto el helio, que sólo posee dos), es decir, tienen completa su última capa.
Afinidad electrónica: La afinidad electrónica (AE) o electroafinidad se define como la energía liberada cuando un átomo gaseoso neutro en su estado fundamental (de mínima energía) captura un electrón y forma un ion mononegativo.
Electronegatividad: La electronegatividad es una medida de la capacidad de un átomo (o de manera menos frecuente un grupo funcional) para atraer a los electrones, cuando forma un enlace químico en una molécula.
Para formar un enlace químico se deben cumplir dos reglas:
La regla del octeto: Los átomos se combinan mediante procesos que implican pérdida, ganancia o compartimiento de electrones de tal forma que adquieran la configuración de ocho electrones en su último nivel; esto se conoce como regla del octeto. Sabemos que los gases nobles tienen ocho electrones en su nivel electrónico más interno (excepto el helio, que sólo posee dos), es decir, tienen completa su última capa.
La regla
del dueto: Cuando
se forma un enlace químico, los átomos reciben, ceden o comparten electrones de
modo que el último nivel de energía de cada átomo contenga 8 electrones y así
adquiera la configuración electrónica del gas noble más cercano en la tabla
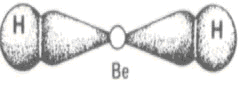
periódica. En el caso de los átomos de los elementos H, Li y Be, cuando
establecen enlaces, tienden a completar su último nivel de energía con 2
electrones y alcanzar la configuración electrónica del gas noble helio (He).
(Regla del dueto)
-Los elementos metálicos ceden electrones.-Los elementos no metálicos ganan o comparten electrones
- Qué diferencia encuentras entre número de oxidación y valencia de un elemento?
Numero de oxidación
Se denomina número de oxidación a la carga que se le asigna a un átomo cuando los electrones de enlace se distribuyen según ciertas reglas un tanto arbitrarias.
Las reglas son:
Los electrones compartidos por átomos de idéntica electronegatividad se distribuyen en forma equitativa entre ellos.
Los electrones compartidos por átomos de diferente electronegatividad se le asignan al más electronegativo.
Luego de esta distribución se compara el número de electrones con que ha quedado cada átomo con el número que posee el átomo neutro, y ése es el número de oxidación. Éste se escribe, en general, en la parte superior del símbolo atómico y lleva el signo escrito.
Valencia
Es el número de electrones que tiene un elemento en su
último nivel de energía, son los que pone en juego durante una reacción química
o para establecer un enlace con otro elemento. Hay elementos con más de una
valencia, por ello se reemplaza a este concepto con el de números de oxidación,
por tanto la valencia es el poder de combinación de los elementos cuando se
unen entre si para formar moléculas.
La etimología de la palabra "valencia" proviene
de 1543, significando "molde", del latín valentia "fuerza,
capacidad", y el significado químico refiriéndose al "poder
combinante de un elemento" está registrado desde 1884, del alemán Valenz.
En 1890, William Higgins publicó bocetos sobre lo que él llamó combinaciones de
partículas "últimas", que esbozaban el concepto de enlaces de
valencia. Si, por ejemplo, de acuerdo a Higgins, la fuerza entre la partícula
última de oxígeno y la partícula última de nitrógeno era 6, luego la fuerza del
enlace debería ser dividida acordemente, y de modo similar para las otras
combinaciones de partículas últimas: estas son las de la tabla periódica.
De acuerdo con los químicos, los electrones de un átomo se configuran alrededor del núcleo, en niveles de energía, órbitas o capas,estas órbitas se representan por letras tales como K, L, M, o por números como 1,2,3
y asi sucesivamente, el numero de electrones presentes en la órbita mas extrema
se conocen como electrones de valencia, y la órbita mas extrema, se denomina
como órbita de valencia.
- Cuales son los diferentes tipos de enlaces que existen definalos y de ejemplos?
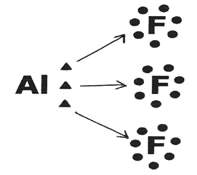
-Enlace
iónico o electrovalente: Se
caracteriza porque hay transferencia de electrones de un átomo a otro, y como
consecuencia se forman iones con cargas eléctricas opuestas, cuya atracción
electrostática da lugar a la formación de correspondiente compuesto químico.
Ejemplo: La sal común se forma cuando los
átomos del gas cloro se ponen en contacto con los átomos del metal
sodio.
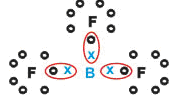
-Enlace
covalente: Es el
que se forma entre dos átomos que tienen la misma electronegatividad o muy próxima,
siendo la diferencia de electronegatividad.
Ejemplo:
El gas cloro está
formado por moléculas, Cl2, en las que dos átomos de cloro se hallan
unidos por un enlace covalente. Enlace covalente de molécula de cloro
Ejemplo:
El enlace
Metálico se presenta en todos los metales si algunas aleaciones por
ejemplo: latón (Cu +Zn), bronce (Cu +Sn), etc.
Mapa conceptual